Niedokrwistość to stan organizmu, który charakteryzuje się obniżeniem stężenia hemoglobiny (Hb) i/lub liczby czerwonych krwinek (RCB). Może być on spowodowany różnymi czynnikami. Do najczęstszych z nich należą: zwiększona utrata krwi, zaburzona erytropoeza i przedwczesny rozpad erytrocytów. Wyróżnia się kilka rodzajów niedokrwistości, w tym makrocytarną niedokrwistość z niedoboru witaminy B12. Jest ona najczęściej konsekwencją schorzenia nazywanego chorobą Addisona-Biermera [1, 2].
Spis treści:
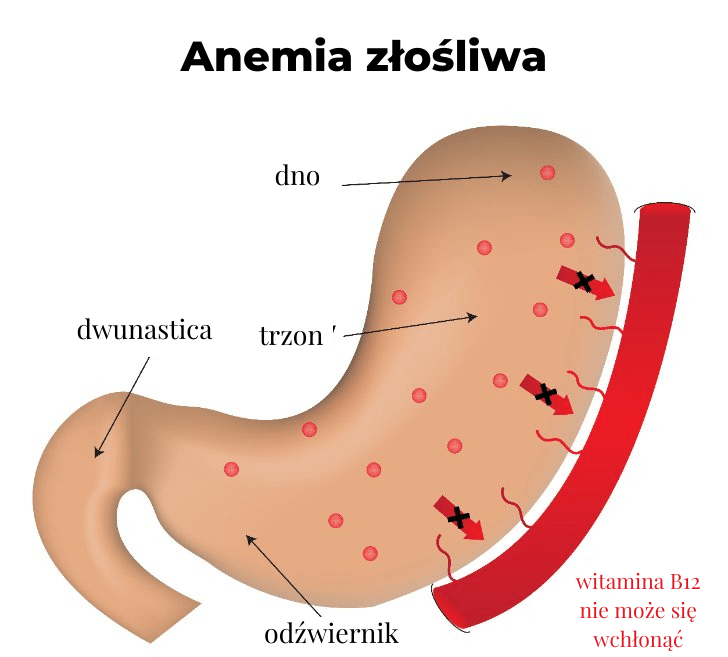
Choroba Addisona-Biermera
Anemia złośliwa (pernicious anemia) to choroba autoimmunologiczna, odznaczająca się niedoborem czynnika Castle’a. Charakterystyczną cechą tego schorzenia jest obecność specyficznych autoprzeciwciał przeciwko komórkom okładzinowym żołądka i/lub czynnikowi wewnętrznemu. W konsekwencji ich działanie uniemożliwia wchłanianie witaminy B12 [5].
Choroba zazwyczaj pojawia się u osób powyżej. 30 roku życia, z podobną częstotliwością u obu płci. Rozpowszechniona jest na całym świecie. W Europie najczęściej rozpoznawana u mieszkańców Skandynawii [6].
Rozpoznanie choroby
Anemię złośliwą diagnozuje się głównie na podstawie testów laboratoryjnych. Do najczęściej wykonywanych badań zaliczamy:
- pełną morfologię krwi
- wykonanie rozmazu krwi obwodowej
- oznaczenie liczby retikulocytów
- zbadanie poziomu witaminy B12, kwasu foliowego oraz żelaza
- wykrywanie autoprzeciwciał przeciwko komórkom okładzinowym żołądka
i czynnikowi IF - badanie szpiku kostnego (w wyjątkowych sytuacjach)
Pomocne może okazać się także zbadanie poziomu gastryny i pepsynogenu. Dodatkowo można rozważyć wykonanie badania histologicznego błony śluzowej żołądka.
Kryteria rozpoznania anemii złośliwej obejmują z kolei:
- stężenie hemoglobiny we krwi <13 g/dL u mężczyzn i <12 g/dL u kobiet
- średnią objętość krwinki (MCV) >100 fL
- niski poziom witaminy B12 w surowicy
wraz z jednoczesną obecnością przeciwciał przeciwko komórkom okładzinowym żołądka/czynnikowi wewnętrznemu.
Należy pamiętać o tym, że diagnostyka choroby Addisona-Biermera często może okazać się trudna, złożona i niejednoznaczna. Dodatkowo wymaga ona także wykluczenia innych przyczyn niedoboru kobalaminy [2, 5, 6, 7].
Objawy
Anemia złośliwa charakteryzuje się niejednolitymi objawami, które mogą pochodzić ze strony różnych narządów oraz układów. Oprócz typowych objawów niedokrwistości takich jak ogólne osłabienie, zaburzenia koncentracji, bóle i zawroty głowy, kołatanie serca mogą wystąpić także inne, mniej specyficzne symptomy. Zaliczamy do nich objawy neurologiczne, wśród których wymienia się drętwienie kończyn, zaburzenia nastroju i obniżoną koordynację ruchową, a także objawy ze strony układu pokarmowego– bóle w nadbrzuszu, wzdęcia, uczucie pełności oraz zapalenie języka. Dodatkowo choroba może współwystępować z infekcjami układu moczowego, a nawet zaburzeniami płodności [5, 7, 8].
Leczenie
Na leczenie choroby Addisona-Biermera składają się dwa aspekty. Po pierwsze, jest to uzupełnianie niedoboru kobalaminy. Najczęściej odbywa się ono poprzez podawanie pacjentom witaminy B12 domięśniowo. Z uwagi na specyfikę choroby, leczenie trwa całe życie. Drugim, równie ważnym punktem terapeutycznym jest monitorowanie efektów leczenia i zapobieganie ewentualnym powikłaniom. Anemii złośliwej może towarzyszyć także niedobór żelaza, dlatego istotne jest obserwowanie poziomu tego pierwiastka we krwi. Oprócz tego nieleczona anemia może w przyszłości prowadzić do zmian nowotworowych żołądka [5, 6, 7, 8].
Możliwy związek z innymi chorobami
Uważa się, że niedokrwistość złośliwa może współistnieć z innymi chorobami autoimmunologicznymi. W badaniach często zauważa się jej związek z autoimmunologicznym zapaleniem tarczycy, cukrzycą typu 1 oraz bielactwem nabytym.
Z tego względu u osób z chorobą Addisona-Biermera uzasadnione może być jednoczesne monitorowanie parametrów charakterystycznych dla wyżej wymienionych chorób [5, 9, 10]
Witamina B12
Jako witaminę B12 (kobalaminę) definiuje się grupę rozpuszczalnych w wodzie związków, które w swojej budowie posiadają centralnie położony jon kobaltu. Aktywność biologiczną witaminy wykazują zarówno formy naturalne, jak również syntetyczne. Różnią się one jednak między sobą właściwościami fizycznymi, takimi jak np. wrażliwość na promieniowanie UV. [3].
Rola w organizmie
Witamina B12 pełni w organizmie szereg istotnych funkcji. Przede wszystkim bierze udział w tworzeniu komórek krwi, w tym także czerwonych krwinek w szpiku kostnym. Oprócz tego odgrywa rolę w powstawaniu DNA i RNA. Co więcej, uczestniczy także w przemianach tłuszczów i węglowodanów oraz aktywacji kwasu foliowego. Dodatkowo odpowiada za prawidłowe funkcjonowanie układu nerwowego. Związane jest to z faktem, że współtowarzyszy ona w budowaniu otoczki mielinowej i tworzeniu przekaźników nerwowych.
Jej niedobór może mieć poważne konsekwencje dla organizmu. Objawiać się on m.in. zaburzeniami neurologicznymi oraz zahamowaniem krwiotworzenia [3, 4].
Źródła i zapotrzebowanie
Źródłem witaminy B12 w diecie są produkty pochodzenia zwierzęcego. Zaliczamy do nich mięso, ryby, jaja, podroby, skorupiaki, a także mleko i jego przetwory. Poza tym dostarczać jej mogą również wzbogacane napoje roślinne (m.in. sojowe, ryżowe, kokosowe). Wchłanialność kobalaminy z diety u zdrowych dorosłych osób utrzymuje się na poziomie 50% [3].
Zapotrzebowanie na witaminę B12 zależne jest m.in. od wieku, płci czy stanu fizjologicznego. Normy polskie opracowane w 2020 roku zalecają dzienną podaż kobalaminy w następującej ilości:
| Grupa płeć, wiek | µg kobalaminy/osobę/dobę | ||
| EAR | RDA | AI | |
| Niemowlęta | |||
| 0-6 miesięcy | – | – | 0,4 |
| 7-11 miesięcy | – | – | 0,5 |
| Dzieci | |||
| 1-3 lat | 0,7 | 0,9 | – |
| 4-6 lat | 1,0 | 1,2 | – |
| 7-9 lat | 1,5 | 1,8 | – |
| Młodzież | |||
| 10-12 lat | 1,5 | 1,8 | – |
| 13-18 lat | 2,0 | 2,4 | – |
| Dorośli | |||
| ≥ 19 lat | 2,0 | 2,4 | – |
| Kobiety w ciąży | 2,2 | 2,6 | – |
| Kobiety w trakcie laktacji | 2,4 | 2,8 | – |
Tab. 1 Opracowanie własne na podstawie Norm Żywienia dla populacji Polski 2020 [3]
Wchłanianie
Witamina B12 wchłaniana jest w końcowym odcinku jelita krętego. Aby jednak proces ten mógł zajść, niezbędna jest obecność glikoproteiny nazywanej czynnikiem wewnętrznym (IF, czynnik Castle’a). Czynnik Castle’a produkowany jest przez komórki okładzinowe żołądka. Ma on za zadanie przetransportować witaminę do odpowiedniego miejsca, tak aby umożliwić jej przyswojenie. W przypadku jego braku lub niewystarczającej ilości transport ten jest zakłócony, a wchłanianie kobalaminy uniemożliwione.
Niedobór czynnika wewnętrznego występuje głównie u pacjentów po przebytym zabiegu usunięcia żołądka oraz w przypadku uszkodzenia błony śluzowej tego narządu. Ponadto jednym ze schorzeń charakteryzującym się upośledzonym wchłanianiem witaminy B12 z powodu braku czynnika IF jest anemia złośliwa, nazywana także chorobą Addisona-Biermera [5].
Dieta przy anemii złośliwej
W przypadku anemii złośliwej dieta nie ma znaczenia terapeutycznego, gdyż niedobór witaminy B12 nie wynika z błędów żywieniowych, tylko zaburzeń wchłaniania. Mimo tego, aby zapobiegać innym niedoborom, a także utrzymywać podstawowe funkcje organizmu ważne jest stosowanie zdrowej i urozmaiconej diety.

W tym celu należy trzymać się podstawowych zasad:
- warzywa i owoce powinny stanowić podstawę diety, a ich dzienne spożycie wynosić minimum 400 g
(z przewagą warzyw nad owocami) - jako źródło węglowodanów należy włączyć do jadłospisu produkty zbożowe
z pełnego przemiału takie jak chleb żytni, płatki owsiane, ryż brązowy czy makaron razowy - codziennym elementem jadłospisu powinny być również produkty będące źródłem białka takie jak chude mięso, ryby, jaja, orzechy, nasiona roślin strączkowych oraz mleko i jego przetwory
- uzupełnienie diety powinna stanowić niewielka ilość tłuszczu pochodzenia roślinnego (np. oliwy z oliwek lub oleju rzepakowego)
Oprócz tego należy pamiętać o odpowiednim nawodnieniu i uprawianiu aktywności fizycznej, a także ograniczeniu spożycia soli, cukru oraz wysoko przetworzonej żywności [11].
Podsumowanie
Anemia złośliwa to choroba autoimmunologiczna, będąca najczęstszą przyczyną niedokrwistości z niedoboru witaminy B12. Charakteryzuje się ona dużą różnorodnością objawów, a jej diagnoza często jest utrudniona. Leczenie choroby trwa całe życie, jednak ważne jest jak najszybsze jego rozpoczęcie. Długotrwały niedobór kobalaminy może mieć poważne i nieodwracalne konsekwencje dla zdrowia. Co więcej, aby zadbać o prawidłowe funkcjonowanie organizmu, chorym zaleca się stosowanie zdrowej diety, dostarczającej wszystkich niezbędnych makroskładników.
Bibliografia:
- Chaparro, C. M., & Suchdev, P. S. (2019). Anemia epidemiology, pathophysiology, and etiology in low- and middle-income countries. Annals of the New York Academy of Sciences, 1450(1), 15–31. https://doi.org/10.1111/nyas.14092
- Oo T. H. (2019). Diagnostic difficulties in pernicious anemia. Discovery medicine, 28(155), 247–253.
- Jarosz, M., Rychlik, E., Stoś, K., & Charzewska, J. (2020). Normy żywienia dla populacji Polski i ich zastosowanie (pp. 68-437). Warsaw, Poland: Narodowy Instytut Zdrowia Publicznego-Państwowy Zakład Higieny.
- Kosmider, A., & Czaczyk, K. (2010). Witamina B12-budowa, biosynteza, funkcje i metody oznaczania. Żywność Nauka Technologia Jakość, 17(5), 17-32.
- Lahner, E., & Annibale, B. (2009). Pernicious anemia: new insights from a gastroenterological point of view. World journal of gastroenterology, 15(41), 5121–5128. https://doi.org/10.3748/wjg.15.5121
- Bizzaro, N., & Antico, A. (2014). Diagnosis and classification of pernicious anemia. Autoimmunity reviews, 13(4-5), 565–568.https://doi.org/10.1016/j.autrev.2014.01.042
- Esposito, G., Dottori, L., Pivetta, G., Ligato, I., Dilaghi, E., & Lahner, E. (2022). Pernicious Anemia: The Hematological Presentation of a Multifaceted Disorder Caused by Cobalamin Deficiency. Nutrients, 14(8), 1672. https://doi.org/10.3390/nu14081672
- Andres, E., & Serraj, K. (2012). Optimal management of pernicious anemia. Journal of blood medicine, 3, 97–103. https://doi.org/10.2147/JBM.S25620
- Zulfiqar, A. A., & Andres, E. (2017). Association pernicious anemia and autoimmune polyendocrinopathy: a retrospective study. Journal of medicine and life, 10(4), 250–253.
- Morawiec-Szymonik, E., Foltyn, W., Marek, B., Głogowska-Szeląg, J., Kos-Kudła, B., & Kajdaniuk, D. (2020). Antibodies involved in the development of pernicious anemia and other autoimmune diseases. Polish archives of internal medicine, 130(1), 31–37. https://doi.org/10.20452/pamw.15094
- https://dietetycy.org.pl/talerz-zdrowia-zalecenia-zdrowego-zywienia-pzh/