Przewód pokarmowy jest największym siedliskiem drobnoustrojów w ciele człowieka. Bakterie i drożdże probiotyczne, bytujące przede wszystkim w jelicie grubym, wykazują korzystny wpływ na zdrowie gospodarza. Mikrobiota jelitowa odgrywa dużą rolę w utrzymaniu właściwego funkcjonowania zarówno układu pokarmowego, jak i układu odpornościowego. Jej ochronne działanie wynika przede wszystkim z konkurencji z patogennymi mikroorganizmami, ze zdolności adhezyjnych do błony śluzowej jelita, z uszczelniania bariery śluzówkowej oraz stymulacji immunologicznej.
Do wzrostu i rozwoju probiotyków niezbędne są składniki odżywcze, które nie są trawione i wchłaniane w jelicie cienkim. Bakterie jelitowe same są zdolne do rozkładu (w precesie fermentacji) i pozyskiwania energii m.in. z polimerów roślinnych. Subtancje te, stymulujące wzrost pożytecznej mikrobioty, zwane są prebiotykami. Produkty metabolizmu tych korzystnych dla zdrowia drobnoustrojów definiowane są zaś jako postbiotyki. One także wykazują szereg działań prozdrowotnych, oddziałowując zarówno miejscowo – w jelicie grubym, jak i ogólnoustrojowo [1,2].
Dysbioza jelitowa
Dysbioza jelitowa, obejmująca nieprawidłowości w składzie i aktywności mikrobioty, obserwowana jest w wielu jednostkach chorobowych, nie tylko w chorobach zapalnych czy czynnościowych jelit, lecz także w chorobach cywilizacyjnych: otyłości i cukrzycy, nowotworach, w schorzeniach autoimmunizacyjnych, jak również w alergiach czy depresji. Na stan mikrobiomu mają też wpływ czynniki, takie jak: rodzaj porodu, karmienie piersią, przebyte antybiotykoterapie oraz stres i dieta [1,3].
Nieprawidłowy skład mikrobiomu może być modulowany przez preparaty probiotyczne lub synbiotyczne, interwencję dietetyczną obejmującą zwiększoną podaż błonnika pokarmowego, którego frakcje w większości zaliczyć możemy do prebiotyków, jak również przez nowo sklasyfikowane postbiotyki [2].
Postbiotyki – definicja i przykłady
Postbiotyki to związki bioaktywne, będące metabolitami bakterii jelitowych. Wśród nich wyróżnia się związki, takie jak: lipidy niskocząsteczkowe – krótkołańcuchowe kwasy tłuszczowe (z ang.: SCFAs – short chain fatty acids), czyli: kwas masłowy, propionowy i octowy; kwasy teichowe, neuropeptydy pochodzące z peptydoglikanu; egzopolisacharydy oraz niższe kwasy organiczne, na przykład kwas mlekowy. Wytwarzane są one najczęściej w procesie fermentacji włókien pokarmowych.
Mikrobiota jelitowa produkuje również szereg innych cząsteczek, w tym witaminy: foliany, witaminę K i B12 oraz metabolity pochodzenia fenolowego (urolitin A, equol i 8-prenylonaringeninę) i aminokwasy aromatyczne. Ze względu na wysoką biodostępność, właściwości przeciwutleniające i sygnalizacyjne, uważa się, że substancje te odgrywają ważną rolę w komunikacji mikrobiom-gospodarz.
Do grupy postbiotyków zaliczane są również paraprobiotyki, które obejmują inaktywowane, czyli nieżywotne komórki drobnoustrojów probiotycznych, a także ich składniki komórkowe: lizaty bakteryjne z białkami powierzchniowymi komórek, fragmenty ścian komórkowych bakterii, antyoksydacyjne enzymy bakteryjne i peptydy [3,4].
Ostatnie badania sugerują, że żywotność bakterii nie jest wymagana w celu osiągnięcia prozdrowotnego działania mikrobiomu jelitowego, lecz to właśnie jego metabolitom i składnikom komórkowym przypisuje się większość działań immunomodulujących. Pozwala to na wykorzystanie postbiotyków we wspomaganiu terapii chorób przebiegających z dysbiozą jelitową lub z zaburzeniami odporności [2-4].
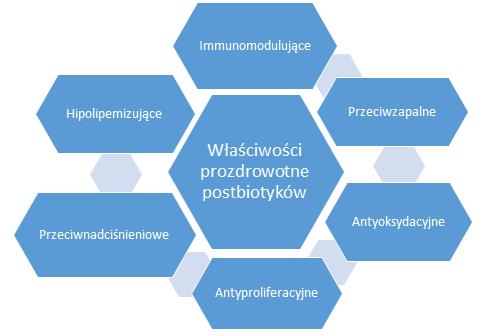
Działanie prozdrowotne postbiotyków
Miejscowo postbiotyki wykazują także działanie antyoksydacyjne, przeciwzapalne oraz przeciwdrobnoustrojowe. Mechanizmy związane z korzystnymi skutkami zdrowotnymi postbiotyków nie są do końca poznane, lecz dane naukowe wskazują na modulację szlaków sygnałowych i metabolicznych, wpływających na wybrane reakcje immunologiczne, neurohormonalne i biochemiczne.

Postbiotyki pełnią prozdrowotne funkcje nie tylko w stosunku do gospodarza, lecz są one także swoistą odżywką dla innych bakterii probiotycznych i stymulują ich prawidłowy rozwój. Działanie to wskazuje na właściwości prebiotyczne postbiotyków, co świadczy o ich ścisłym powiązaniu w mikrobiomie jelitowym.
Efekty ogólnoustrojowe komponentów komórkowych bakterii probiotycznych lub ich metabolitów, opisane w badaniach in vitro lub na modelu zwierzęcym, obejmują działanie przeciwnadciśnieniowe, hipocholesterolemiczne, antyproliferacyjne w stosunku do komórek nowotworowych jelita grubego i przeciwdziałające otyłości, polegające na obniżeniu aktywności prozapalnej tkanki tłuszczowej i zmniejszeniu nietolerancji glukozy. Opisana została także rola hepatoprotekcyjna postbiotyków, polegająca m.in. na obniżeniu markerów stresu oksydacyjnego i odnawianiu poziomu glutationu [5].
Bezpieczeństwo stosowania i przewaga postbiotyków nad probiotykami
Stosowanie probiotyków w określonych sytuacjach klinicznych nie jest zalecane przez ekspertów, gdyż podanie żywych bakterii osobom z osłabionym układem immunologicznym (m.in. wcześniakom, niemowlętom, chorym z zaburzeniami odporności) może nieść za sobą niekorzystne implikacje. Skutki uboczne niewłaściwego zastosowania probiotyku mogą dotyczyć: dolegliwości żołądkowo-jelitowych, translokacji bakteryjnej z nadmiernym rozrostem flory jelitowej czy przeniesienia genów odporności na antybiotyki między bakteriami probiotycznymi a patogennymi.
Postbiotyki niosą tylko fragmenty komórkowe owych unieczynnionych już bakterii lub ich metabolity, co pozwala nam uniknąć ryzyka działań niepożądanych przy utrzymaniu korzyści prozdrowotnych. Dodatkowym atutem postbiotyków jest ich długa trwałość (nawet do 5 lat) i stabilność w produktach spożywczych czy suplementach diety oraz łatwa przyswajalność z preparatów leczniczych.
Stosowanie postbiotyków może stanowić bezpieczniejszą alternatywę dla probiotyków, a w przyszłości stać się wiodącą strategią w leczeniu chorób przebiegających z dysbiozą jelitową czy zaburzeniami odporności [5].
Zastosowanie kliniczne postbiotyków
Krótkołańcuchowe kwasy tłuszczowe (z ang.: SCFA – short chain fatty acids): kwas masłowy, kwas propionowy i kwas octowy, należą do najbardziej znanych postbiotyków. Kwas masłowy jest podstawowym źródłem energii dla kolonocytów, czyli komórek nabłonkowych jelita grubego. Wykazuje również działanie przeciwzapalne i regenerujące na błonę śluzową jelita, co zapobiega jej zwiększonej przepuszczalności. Kwas masłowy, w postaci dietetyczego środka spożywczego o specjalnym przeznaczeniu medycznym, stosowany jest w terapii nieswoistych chorób zapalnych jelit, takich jak: choroba Leśniowskiego-Crohna czy wrzodziejące zapalenie jelita grubego, w biegunkach różnego pochodzenia, w zespole jelita nadwrażliwego, w chorobie uchyłkowej czy u osób z zaburzeniami odporności, osłabionych, przewlekle chorych. SCFA posiadają również inne korzystne działania metaboliczne, takie jak: regulacja gospodarki lipidowej (obniżenie cholesterolu całkowitego w surowicy krwi) i wyrównanie homeostazy węglowodanowej (zwiększenie insulinowrażliwości tkankowej) [1,5].
Paraprobiotyki, czyli inaktywowane wysoką temperaturą szczepy probiotyczne, wykazują większą stabilność w układzie trawiennym człowieka w porównaniu do probiotyków. Wszystkie badania z wykorzystaniem postbiotyków u dorosłych oparte są na produktach pochodzących z nieżywotnych gatunków bakterii mlekowych i potwierdzają ich bezpieczeństwo. Udowodniono, że posiadają one właściwości immunomodulujące, które polegają na wywoływaniu reakcji układu odpornościowego w odpowiedzi na elementy komórkowe drobnoustrojów. Z tego względu preparaty zawierające paraprobiotyki mogą być traktowane jako immunobiotyki. Stwierdzono, że postbiotyk Lactobacillus pentosus b240 może zmniejszać, zależnie od dawki, częstość przeziębienia u osób starszych. Lactobacillus acidophilus LB wykazuje pozytywny wpływ na funkcjonowanie przewodu pokarmowego oraz w leczeniu przewlekłej biegunki lub zespołu jelita nadwrażliwego (z ang.: IBS – irritable bowel syndrome) z przewagą biegunki, redukując częstość wypróżnień [4]. Podawanie tego postbiotyku skutkowało znaczącym skróceniem czasu biegunki związanej z ostrym zapaleniem żołądka i jelit u dzieci [1,4,6].
Mieszanki dla niemowląt oparte na mleku fermentowanym (z ang: FIFs – fermented infant formulas) również wpisują się w definicję postbiotyku. Preparaty te poddawane są fermentacji z udziałem bakterii wytwarzających kwas mlekowy lub innymi bakteriami, i w większości przypadków nie zawierają żywych bakterii. Badania potwierdzają, że zastosowanie FIFs jest bezpieczne w użyciu i dobrze tolerowane przez noworodki i wcześniaki.
Postbiotyki pochodzące z Bifidobacterium breve C50 i Streptococcus thermophilus 065, często także w połączeniu z oligosacharydami prebiotycznymi w mieszankach dla niemowląt wykazały: działanie łagodzące kolek niemowlęcych, rzadzsze występowanie biegunek, wzdęć brzucha i regulację konstyntencji stolca, zmniejszenie stężenia kalprotektyny i markerów zapalnych w kale, obniżenie ryzyka infekcji pokarmowych i oddechowych, wzrost poziomu bifidobakterii, a także potencjalne korzyści w leczeniu ostrej biegunki – skrócenie czasu jej trwania. Inni autorzy nie zaobserwowali istotnych różnic w zapobieganiu czy leczeniu biegunek przy stosowaniu B. breve C50 i S. thermophilus 065 w porównaniu ze standardowym mlekiem modyfikowanym dla niemowląt.
Stwierdzono, że Lactobacillus paracasei CBA L74 może zapobiegać powszechnym chorobom zakaźnym u małych dzieci i pozytywnie modulować mikrobiotę jelitową poprzez wzrost liczebności bakterii probiotycznych produkujących maślan. Zaobserwowano także zmniejszenie zaburzenia wchłaniania laktozy u dzieci z nietolerancją tego dwucukru po podaniu zarówno żywych, jak i inaktywnowanych cieplnie komórek Lactobacillus paracasei 33. Połączone wyniki dwóch badań randomizowanych profilaktycznych wykazały, że inaktywowana cieplnie L. paracasei CBA L74 zmniejszała ryzyko biegunki o 49%, zapalenia gardła o 69% i zapalenia krtani o 56% w porównaniu z placebo u małych dzieci. Nie stwierdzono istotnych różnic w ryzyku wystąpienia nieżytu nosa czy zapalenia ucha środkowego [4,6].
Wyniki przytoczonych badań są jednak niewystarczające, aby rutynowo zalecać stosowanie wybranych postbiotyków w leczeniu biegunki lub wspomaganiu odporności u niemowląt karmionych sztucznie czy u starszych dzieci. Konieczne są dalsze badania randomizowane na dużej grupie badanych w celu ustalenia skutków działania i bezpieczeństwa stosowania różnych postbiotyków [6].
Postbiotyki jako terapia wspomagająca leczenie lub prewencja chorób
1) Choroby czynnościowe i zapalne jelit
Stosowanie postbiotyków może być skuteczne w regulacji rytmu wypróżnień, zarówno zapobieganiu biegunkom z różnych przyczyn, jak i we wspomaganiu funkcji perystaltycznych jelit. Wykazano, że inaktywowany termicznie Lactobacillus gasseri CP2305, będący składnikiem fermentowanego mleka, reguluje pracę dolnego odcinka przewodu pokarmowego, a także zmniejsza objawy żołądkowo-jelitowe oraz poziom chronicznego zmęczenia związanego ze stresem, co może być wykorzystane w terapii zespołu jelita nadwrażliwego (z ang. IBS – irritable bowel syndrome) [7].
Wykazano, że podanie pacjentom z IBS inaktywowanego szczepu Lactobacillus LB skutkuje zmniejszeniem poziomu bólu oraz redukcją wzdęć i liczby luźnych stolców po miesięcznym stosowaniu [4].
🔎 Postbiotyki, głównie z bakterii Lactobacillaceae i Bifidobacteriaceae, wykazują działanie przeciwzapalne poprzez regulację cytokin i wzmocnienie bariery jelitowej. Mogą wspierać terapię w chorobach autoimmunologicznych, IBD i zespole metabolicznym [16].
Sugeruje się, że krótkołańcuchowe kwasy tłuszczowe oraz tryptofan mogą mieć immunomodulujący wpływ w chorobach zapalnych jelit. Poprzez regulację komórek odpornościowych SCFAs zmniejszają stan zapalny, co ważne jest w utrzymaniu remisji [8].
2) Choroby metaboliczne
W badaniach klinicznych potwierdzono korzystny wpływ na funkcje metaboliczne wielu szczepów inaktywowanych bakterii probiotycznych. Przykładowo L. reuteri GMNL-263, stosowany przez 3 miesiące, powodował obniżenie insulinooporności tkankowej i poziomu glukozy we krwi oraz redukował stuszczenie wątroby. W badaniach na modelach zwierzęcych, postbiotyki, takie jak: wewnątrzkomórkowe organella L. casei CRL431, egzopolisacharydy B. animalis RH i Lact. lactis subsp. lactis zwiększały pojemność antyoksydacyjną osocza, stężenie enzymów przeciwutleniających oraz zmniejszały peroksydację lipidów w wątrobie i w osoczu krwi [9].
3) Atopowe zapalenie skóry
Podawanie przez 12 tygodni preparatu z unieczynnionym Lactobacillus paracasei K71 skutkowało zmniejszeniem intensywności i powierzchni chorobowych zmian skórnych u osób z łagodnym bądź umiarkowanym atopowym zapaleniem skóry [9].
4) Infekcja Helicobacter pylori
W badaniach wykazano, że paraprobiotyk zawierający nieżywotny Lactobacillus reuteri DSMZ 17648, okazał się skuteczny w zwalczaniu H. Pylori [9].
5) Nowotwór jelita grubego
Wiele postbiotyków i paraprobiotyków, pozyskiwanych m.in. z Lactobacillus spp. wykazuje działanie antyproliferacyjne i apoptotyczne w stosunku do linii komórkowych raka jelita grubego (badania in vitro). Ich mechanizm działania obejmuje wpływ na ekspresję genów regulatorowych, immunomodulację (zmniejszenie stanu zapalnego jelit i wzmocnienie bariery śluzówkowej) oraz unieszkodliwianie substancji kancerogennych pochodzących z żywności [10].
6) Alergie pokarmowe
Dzięki właściwościom immunomodulującym postbiotyków sugeruje się, że mogą być one stosowane w celu prewencji alergii pokarmowych. SCFAs, przyczyniając się do zwiększenia integralności błony śluzowej jelit, uniemożliwiają transmisję potencjalnych alergenów do wnętrza organizmu [11].
W badaniu na modelu zwierzęcym zaobserwowano zmniejszenie endotoksemii bakteryjnej (obniżenie stężenia lipopolisacharudu – LPS) po podaniu postbiotyku w postaci bezkomórkowego supernatantu bakterii probiotycznej Lactobacillus reuteri ZJ617, co świadczy o zmniejszeniu przesiąkliwości jelit, biorącej udział w patogenezie alergii [12].
7) Odporność na zatrucia pokarmowe
🔎 Postbiotyki, jako produkty metaboliczne probiotyków, wykazują właściwości antybakteryjne i przeciwutleniające, które mogą hamować rozwój patogenów takich jak Staphylococcus aureus, Salmonella enterica i Escherichia coli, oraz zapobiegać chorobom związanym ze stresem oksydacyjnym. Ich zastosowanie w funkcjonalnej żywności przyczynia się do poprawy zdrowia jelit i zmniejszenia ryzyka chorób przenoszonych przez żywność [14].
Zastosowanie w dietetyce sportowej
🔎 Postbiotyki mogą wspierać nastrój, zmniejszać zmęczenie i zwiększać gotowość sportowców do treningu, chociaż potrzebne są dalsze badania, aby zrozumieć ich wpływ na zdrowie, wydolność i regenerację [15].
Przyszłość postbiotyków w żywności funkcjonalnej
Wygodną do stosowania i najskuteczniej działającą formą postbiotyków są tabletki lub kapsułki w postaci suplementu diety lub dietetycznego środka spożywczego o specjalnym przeznaczeniu medycznym (zawierające paraprobiotyki lub metabolity bakteryjne), które powoli wchodzą na polski rynek farmaceutyczny. Ich stosowanie powinno być poparte jednak zaleceniem lekarskim w wybranych przypadkach klinicznych, a czas trwania kuracji należy dopasować do potrzeb pacjenta (badania kliniczne opierają się zazwyczaj o wyniki 3-miesięcznych interwencji).
Różnego rodzaju produkty spożywcze również mogą stanowić nośnik dla postbiotyków. Najczęściej w tym celu wykorzystywane są fermentowane mleko oraz jego przetwory, zakwaszane pałeczkami kwasu mlekowego, które następnie inaktywuje się ciepłem. Produkty te wpisują się w konwencję żywności funkcjonalnej, która posiada nie tylko wartości odżywcze, ale także wykazuje działanie prozdrowotne przy zwyczajowym spożyciu.
Fermentowane napoje mleczne nie są jedyną grupą produktów spożywczych mogących dostarczać postbiotyki z diety. Produkty spożywcze pochodzenia zbożowego lub warzywnego, poddane fermentacji mlekowej, także znajdą tutaj zastosowanie, zwłaszcza dla osób na diecie bezmlecznej lub wegańskiej. Wyróżniają się one również dużą zawartością witamin z grupy B, wspieraną przez syntezę bakteryjną, a także zwiększoną biodostępnością wapnia, żelaza i cynku z tych produktów oraz niższym stężeniem fitynianów i gliadyny w porównaniu z produktami niefermentowanymi. Obróbka termiczna, której poddawane są fermentowane produkty zbożowe (np. pieczywo na zakwasie), inaktywuje żywe bakterie, przy zachowaniu postbiotycznych właściwości [4].
Istnieje duże prawdopodobieństwo, że w niedalekiej przyszłości postbiotyki staną się pożądanym składnikiem żywności funkcjonalnej. Obecnie jednak w naszym kraju produkty postbiotyczne są rzadko lub nie są powszechnie dostępne.
W celu wsparcia swojego mikrobiomu jelitowego do producji postbiotyków, należy dostarczać organizmowi źródła pokarmowe, które są ich prekursorami. Należą do nich przede wszystkim błonnik pokarmowy, zawarty w pełnoziarnistych produktach zbożowych, orzechach, nasionach roślin strączkowych, warzywach i owocach, prebiotyki – np. oligosacharydy i inulina, występujące w cykorii, cebuli czy soi, a także polifenole – związki bioaktywne żywności roślinnej, których największe koncentracje znajdziemy w kakao, herbacie, ziołach i przyprawach oraz w wybranych owocach i warzywach. Różnorodność produktów spożywczych i mało przetworzona żywność to podstawa diety korzystnej dla mikrobiomu jelitowego [13].
Podsumowanie
Postbiotyki mogą wywierać korzystny efekt zdrowotny dla człowieka poprzez modulację mikrobiomu jelitowego oraz wsparcie układu immunologicznego. Ich obecne zastosowanie obejmuje przede wszystkim mieszanki dla niemowląt oparte na mleku fermentowanym oraz dietetyczne środki spożywcze o specjalnym przeznaczeniu medycznym zawierające paraprobiotyki lub metabolity bakterii probiotycznych. W badaniach potwierdzono ich działanie immunomodulujące, przeciwzapalne i przeciwdrobnoustrojowe, co pozwala na ich wykorzystanie w terapii chorób zapalnych jelit, biegunek czy innych chorób przebiegających z dysbiozą jelitową lub z zaburzeniami odporności. Potrzeba jednak wielu badań klinicznych nad mechanizmem działania postbiotyków i ich skutecznością w wybranych schorzeniach u ludzi, aby stały się one częścią postępowania leczniczego i wkroczyły na rynek jako nowy rodzaj żywności funkcjonalnej.
Piśmiennictwo
- Ruszkowski, J., Szewczyk, A., & Witkowski, J. M. (2018). Przegląd doustnych prebiotyków, probiotyków, synbiotyków i postbiotyków dostępnych na polskim rynku aptecznym. Farm Pol, 74(2), 114-122.
- Tomasik, P., & Tomasik, P. (2020). Probiotics, non-dairy prebiotics and postbiotics in nutrition. Applied Sciences, 10(4), 1470.
- Żółkiewicz, J., Marzec, A., Ruszczyński, M., & Feleszko, W. (2020). Postbiotics—A Step Beyond Pre-and Probiotics. Nutrients, 12(8), 2189.
- Wegh, C. A., Geerlings, S. Y., Knol, J., Roeselers, G., & Belzer, C. (2019). Postbiotics and their potential applications in early life nutrition and beyond. International journal of molecular sciences, 20(19), 4673.
- Aguilar-Toalá, J. E., Garcia-Varela, R., Garcia, H. S., Mata-Haro, V., González-Córdova, A. F., Vallejo-Cordoba, B., & Hernández-Mendoza, A. (2018). Postbiotics: An evolving term within the functional foods field. Trends in Food Science & Technology, 75, 105-114.
- Malagón-Rojas J., Mantziari A., Salminen S., Szajewska H.: Postbiotics for Preventing and Treating Common Infectious Diseases in Children: A Systematic Review. Nutrients 2020, 12 (2): 389
- Barros, C. P., Guimarães, J. T., Esmerino, E. A., Duarte, M. C. K., Silva, M. C., Silva, R., … & Cruz, A. G. (2020). Paraprobiotics and postbiotics: Concepts and potential applications in dairy products. Current Opinion in Food Science, 32, 1-8.
- Russo, E., Giudici, F., Fiorindi, C., Ficari, F., Scaringi, S., & Amedei, A. (2019). Immunomodulating activity and therapeutic effects of short chain fatty acids and tryptophan post-biotics in inflammatory bowel disease. Frontiers in Immunology, 10.
- Cuevas-González, P. F., Liceaga, A. M., & Aguilar-Toalá, J. E. (2020). Postbiotics and Paraprobiotics: From concepts to applications. Food Research International, 109502.
- Rad, A. H., Aghebati-Maleki, L., Kafil, H. S., & Abbasi, A. (2020). Molecular mechanisms of postbiotics in colorectal cancer prevention and treatment. Critical Reviews in Food Science and Nutrition, 1-17.
- Homayouni Rad, A., Aghebati Maleki, L., Samadi Kafil, H., & Abbasi, A. (2020). Postbiotics: A novel strategy in food allergy treatment. Critical Reviews in Food Science and Nutrition, 1-8.
- Anderson, R. C. (2019). Are Postbiotics the Long Sought-After Solution for a Leaky Gut?. The Journal of nutrition, 149(11), 1873-1874.
- Klemashevich, C., Wu, C., Howsmon, D., Alaniz, R. C., Lee, K., & Jayaraman, A. (2014). Rational identification of diet-derived postbiotics for improving intestinal microbiota function. Current Opinion in Biotechnology, 26, 85-90.
- https://onlinelibrary.wiley.com/doi/10.1155/2024/1868161
- Kerksick CM, Moon JM, Jäger R. It’s Dead! Can Postbiotics Really Help Performance and Recovery? A Systematic Review. Nutrients. 2024 Mar 1;16(5):720. doi: 10.3390/nu16050720. PMID: 38474848; PMCID: PMC10933997.
- Zdybel K, Śliwka A, Polak-Berecka M, Polak P, Waśko A. Postbiotics Formulation and Therapeutic Effect in Inflammation: A Systematic Review. Nutrients. 2025 Jun 30;17(13):2187. doi: 10.3390/nu17132187. PMID: 40647290; PMCID: PMC12251375.
- Data pierwotnej publikacji: 30.09.2020
- Data ostatniej aktualizacji o wyniki badań: 6.08.2025